| PREVENCIÓN | GAS ACETILENO |
| PROGRAMAS AUDIOVISUALES PARA LA PREVENCIÓN DE INCENDIOS | |
DIAPOSITIVA TEXTO
 |
1 Iniciación del programa |
 |
2 El acetileno se compone de carbono e hidrógeno, formando sus moléculas un triple enlace químico que es causa de su reactividad. Es un gas combustible, no tóxico, incoloro e inodoro s¡ bien posee un olor característico debido a las impurezas que se producen en su composición. |
 |
3 Se obtiene haciendo reaccionar con agua un compuesto del carbono y del calcio, conocido como carburo de calcio. Actualmente también se puede conseguir partiendo del gas metano. |
 |
4 La llama que produce el acetileno, es blanca rojiza ofreciendo gran luminosidad. A principios de siglo fue muy utilizado para el alumbrado en las conocidas lámparas de carburo hasta que fue desplazado por la electricidad. |
 |
5 Su límite de inflamabilidad es muy amplio en comparación con otros gases de uso común. Con el aire ambiente, es inflamable en una proporción de 2,5 a 81% lo que le confiere un mayor riesgo ante fugas incontroladas. |
 |
6 Su principal riesgo se encuentra en su inestabilidad. El gas acetileno es un gas inestable que reacciona químicamente ante cualquier agresión como puede ser: elevando su presión, elevando su temperatura, por percusión o por incompatibilidades con algunas metales puede llegar a explotar. |
 |
7 Debido el triple enlace que presenta su estructura molecular, el acetileno se halla en constante tensión. A presión y temperatura ambiente este tensión no es suficiente para originar su descomposición o polimerizaci6n. |
 |
8 Pero tan solo elevando la presión del gas por encima de una atmósfera y media, la tensión ya es suficiente para iniciar la descomposición en sus elementos, lo que se realiza con desprendimiento de calor. |
 |
9 También una elevación de su temperatura por encima de los 120 grados es suficiente para iniciar la polimerización, lo que también se realiza con desprendimiento de calor. Ambas reacciones siguen un proceso acelerado que finalmente es explosivo |
|
|
10 El acetileno se puede licuar con facilidad, igual que se hace con el gas butano en las bombonas, pero su inestabilidad en estado líquido lo hace fácilmente explosivo. |
 |
11 El acetileno es incompatible con algunos metales como la plata, el cobre o el mercurio, en contacto con los mismos produce acetiluros de tipo pulverulento los cuales son altamente explosivos. |
 |
12 Para poder comercializar el acetileno a presiones superiores a dos kilos de forma que ofreciera unas garantías de seguridad, fue necesario construir un recipiente de especiales características capaces de frenar su inestabilidad y fácil descomposición. |

|
13 Al principio se comprobó que la acetona es el mejor disolvente del acetileno, por lo cual el gas se podía mantener disuelto en acetona elevando su presión sin riesgo. |
 |
14 El acetileno queda disuelto en la acetona de igual forma que el gas carbónico se disuelve en el agua dentro de un sifón o cualquier bebida gaseosa. |
 |
15 La acetona actúa como pacificadora de las moléculas que por la presión tienden a chocar y rechazarse lo que es causa de su descomposición con elevación progresiva de la temperatura. La acetona envuelve a las moléculas de acetileno formando un mullido cojín que las separa entre si, evitando la tensión de su contacto directo. |

|
16 El sistema se perfecciono llegando al envase actual que consigue mayor aislamiento de las moléculas al estar cubierto su interior por una masa neutra y porosa que impide que sobre la superficie de la acetona puede existir acetileno a presión elevada, de tal forma que se anula prácticamente el riesgo de reacción. |
 |
17 Este material poroso que ocupa del 80 al 90% de la capacidad total de la botella, puede compararse con une gran esponja sólida, llena de pequeñísimas cavidades que se comunican entre si. Esta compuesta por diferentes substancias según patentes de los fabricantes |
 |
18 La materia porosa ayuda a la acetona, de forma que cada poro actúa como recipiente independiente de presión, separando en distintas cavidades a pocas moléculas disueltas en acetona, lo que permite que sean cargadas y comercializadas las botellas con suficientes garantías de seguridad. |
 |
19 Una botella de acero de acetileno de 40 litros de capacidad queda reducida a 30 litros una vez dotada del relleno poroso. Para impregnar la substancia porosa se la añaden 16 litros de acetona que permiten la disolución de 6.000 litros de acetileno a 15 atmósferas de presi6n, con lo cual aun quedan 4 litros de capacidad para compensar dilataciones de la acetona por cambios de temperatura exterior. |
 |
20 Las botellas llevan marcadas en el exterior la tara, que corresponde a la suma de envase, más relleno poroso más acetona, pudiendo conocer el contenido de gas por pesada, contando que un metro cúbico de gas en condiciones normales pesa un kilo ciento diez gramos. |
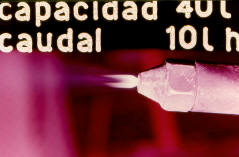 |
21 Cuando se consume gas de una botella de acetileno siempre se produce un arrastre de gotas de acetona, para evitar que este sea excesivo nunca se debe sobrepasar un caudal equivalente a la cuarta parte de la capacidad de la botella, es decir, para una botella de 40 litros de capacidad, el caudal máximo de consumo será de diez litros hora. |
 |
22 Para evitar un arrastre excesivo de acetona, las botellas de acetileno deben utilizarse en posición vertical o como máximo recostadas de forma que la ojiva quede un metro más alta que la base. |
 |
23 Se recomienda no exponerlas al sol ni cerca de una fuente de calor. Como ya sabemos, con el calor todos los gases aumentan de presión y con el acetileno este acción es doblemente peligrosa. El calor disminuye la viscosidad de la acetona mientras la presión aumenta, lo que facilita la tensión en sus moléculas. |
 |
24 Se ha de evitar que las botellas estén sometidas a vibraciones ya que el rozamiento de la masa porosa con la pared interior de la botella produce un calor suficiente para alejar la acetona del acetileno dejando a este libre para reaccionar. |
|
25 Los mismos efectos pueden ocurrir si las paredes del cilindro reciben un golpe, como puede ser la caída de la botella contra el suelo. El impacto puede iniciar la polimerización aunque las condiciones de acetona y masa porosa sean correctas en la botella. Una vez iniciada la reacción exotérmica, se va elevando la temperatura hasta llegar a poner la botella al rojo y hacerla estallar. |
 |
26 Por ello es necesario que en el lugar de trabajo las botellas estén sujetas o bien montadas en carretillas porta botellas especialmente diseñadas para el transporte de las mismas, con fijaciones que evitan un posible vuelco. |
 |
27 Otra posible causa de descomposición del gas, puede ser el retroceso de la llama hacia el interior de la botella. Esta se puede producir entre otras causas al dilatarse la boquilla del soplete por exceso en el tiempo de trabajo obturando la salida del gas. |
 |
28 0 por tocar con la boquilla del soplete la pieza que se está cortando a soldando, por presiones inadecuadas de trabajo a por comunicación en el mezclador situado en el soplete por falta de un periódico mantenimiento. |
 |
29 Puede suceder que después de un chasquido seco, el soplete se apague oyendo seguidamente un silbido en el interior del soplete al tiempo que aparece una llama puntiaguda y humeante, ello indica que se ha producido un retroceso de llama hacia la botella. |
 |
30 El retroceso de llama puede ser más escandaloso al explosionar la tubería flexible saliendo llamas de la misma, siendo la causa la entrada de oxigeno a presión elevada en la tubería de acetileno de menor resistencia |
 |
31 Para evitar tales casos existen válvulas anti retroceso de llama que se deben colocar siempre en las salidas de los manoreductores de oxigeno y de acetileno, pues el retroceso de llama también puede producirse hacía le botella de oxígeno. |
 |
32 Cuando las mangueras tengan una longitud superior a tres metros, deberán instalarse además válvulas anti retroceso complementarías a la entrada de oxigeno y acetileno en el soplete o entre gomas a un metro de distancia de este según los casos. |
 |
33 La forma de actuar ante un retroceso de llama consistirá en cerrar inmediatamente la botella de oxigeno y la de acetileno aunque se disponga de válvulas anti retroceso, para la cual es necesario que la llave de cuadradillo del grifo de acetileno este siempre puesta en su alojamiento. |
 |
34 Ante cualquier tipo de anomalía siempre se cerrará la botella. Si la ubicación de la botella o las llamas no permiten el acceso para cerrar la salida de gas, se podrá extinguir fácilmente empleando un extintor de polvo seco, o C02 dirigiendo el chorro el inicio de las llamas y en dirección de las mismas. |
 |
35 Una vez sofocadas las llamas y cerrada la botella se avisará inmediatamente el suministrador. Se comprobará con la palma de la mano la temperatura de la botella y si se observa que está caliente y que esta temperatura va en aumento... |

|
36 Se ha de refrigerar la botella empleando gran cantidad de agua sin moverla de donde se encuentre, los síntomas indican que se ha iniciado la descomposición y solo el frío producido por el agua es capaz de frenarla. |
 |
37 Sí la polimerización está avanzada, la botella desprenderá vapor indicando su temperatura elevada, en este caso la refrigeración se realizará desde lugares protegidos desde la máxima distancia que permitan las mangueras. |
 |
38 Después de unos veinte minutos de refrigerar con agua sin que se observe vapor, se podrá comprobar de nueva la temperatura con la palma de la mano |
 |
39 Se ha de refrigerar con agua durante el tiempo que sea necesario hasta que la botella quede completamente fría, después se tendrá en observación comprobando continuamente su temperatura, S¡ se mantiene fría durante 90 minutos sin refrigerarla se podrá trasladar con cuidado hasta un deposito o bidón con agua donde se introducirá. |
 |
40 En todos los casos se recomiende cerrar la botella de acetileno, cuando lo lógico sería abrirla para eliminar el aumento de presión. Cualquier recipiente que contenga líquidos o gases con peligro de explosión por exceso de presión, eliminando la presión al abrir el grifo desaparece el el riesgo |
 |
41Con el acetileno no ocurre así, quizás esta tabla pueda explicar la que sucede en el interior de la botella cuando por diversas causas se inicia la polimerización. El primer dibujo muestra las causas que pueden iniciar la descomposición En el segundo la polimerización continua de forma progresiva, la botella empieza a estar caliente. La tercera botella muestra la reacción exotérmica, las moléculas cercanas el centro de reacción van sumándose a la misma, al tiempo que la acetona se aparte del calor facilitando que la reacción aumente. En el cuarto dibujo ya se ha creado un espacio vacío de acetona. Se produce la destrucción de parte de la masa porosa, la temperatura y la presión son muy elevadas, dejándola en estas condiciones llegaría e explotar Sin embargo la refrigeración con gran cantidad de agua consigue reducir la temperatura y en consecuencia la presión. La reacción se va amortiguando hasta detenerse, la acetona retorna a la zona afectada. Han transcurrido 90 minutos sin emplear agua y no se aprecia temperatura en la botella. En la zona dañada existen gases inactivos como hidrógeno y partículas de carbón a igual presión que el resto de la botella . . . El peligro principal ya ha pasado. |
 |
42 No obstante se ha de manejar con cuidado, un golpe seco podría desplazar la masa porosa haciendo que la zona afectada reaccionara a gran velocidad haciendo estallar la botella al instante. |
 |
43 Ahora veamos lo que puede ocurrir en el mismo caso pero actuando de forma incorrecta. El empleo de agua es correcto, pero al abrir la válvula de salida con la intención de reducir la presión, se está creando una corriente de gas hacia el exterior. Las moléculas de acetileno fluyen hacia la salida atravesando el centro de reacción en donde aumentan su temperatura y el salir de este forman otro u otros centros de polimerización. Cuanto mayor sea la salida de gas más rápida será le reacción, multiplicándose sin que el agua en este caso de aceleración puede llegar a frenarla. |
 |
44 Hubo un tiempo en que se consideraba adecuado abrir la válvula ligeramente para dejar escapar la presión excesiva, hasta el extremo que exíste un país donde están normalizadas las botellas con pequeñas válvulas de escape en la parte baja. No obstante el hollín y las partículas desprendidas por la descomposición obturan la salida después de haber aumentado la reacción. |
 |
45 Alrededor de un 15% de los accidentes graves que se producen en los equipos de soldadura, provienen de fallos en las tuberías flexibles por desgaste o cortes en las mismas, de ahí que deban tomarse toda clase de precauciones en cuanto a la calidad, conservación y sujeción de las mismas, tales como.. |
 |
46 Para limitar las consecuencias de la posible inflamación de una fuga en las tuberías flexibles, se evitará llevar las mangueras sobre la espalda, hacerlas pasar entre las piernas o mantenerlas enrolladas alrededor de las botellas especialmente mientras se esta trabajando. |
 |
47 Para evitar confusiones, siempre debe emplearse la tubería roja (en algún caso verde) para el gas combustible y la azul para el oxigeno. |
 |
48 Las tuberías flexibles se unirán a las válvulas anti retroceso de llama situadas en los manoreductores y en el soplete sujetándolas mediante abrazaderas adecuadas. No se utilizaran ligadas con alambre, ni se intentará corregir una fuga mediante cinta aislante, |
 |
49 Para localizar una posible fuga se empleará agua jabonosa o bien se introducirá la manguera en un recipiente con agua, nunca se empleará una llama. |
 |
50 Se evitará arrastrar por el suelo los flexibles, dejarlos de forma que los alcancen las chispas del propio trabajo a hacerles atravesar zonas de paso sin la adecuada protección. |
 |
51 Nunca debe estrangularse una manguera para cortar el paso de gas, por ejemplo para cambiar el soplete o la boquilla del mismo, pues aparte de dañar le tubería no existe una certeza de cierre. |
 |
52 En el caso de producirse inflamación de una eventual fuga en el manoreductor, se actuará de forma que el operario no se coloque delante de la llama pues esta puede aumentar de tamaño inesperadamente y lesionarse. Si la llama impide cerrar la botella se emplearé un extintor. |
 |
53 Cuando se precise empalmar dos tramos de tubería flexible, se emplearán accesorios de bronce, nunca de cobre. Los metales con aleaciones que tengan más de un 60% de cobre corren el riesgo de formar acetiluros. |
 |
54 Una vez vacías, las botellas de acetileno continuaran estando llenas de acetona, por lo cual merecen las mismas precauciones, teniendo de almacénarse con la válvula cerrada y el capuchón roscado, lejos de cualquier fuente de calor. |
 |
55 En el soplete arde gas acetileno con el aire ambiente, la llama es blanca y humeante teniendo en estas condiciones pocas aplicaciones prácticas. Para conseguir una combustión adecuada y máxima temperatura precisa mezclarse con oxigeno a presión. |
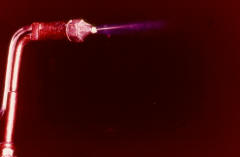 |
56 El oxigeno "limpia" la llama, ajustando adecuadamente los grifos del soplete, la mezcla inflamable produce un brillante dardo de fuego capaz de superar los 3.I00 grados centígrados de temperatura. |
 |
57 El hierro, el acero y la mayoría de metales se transforman en miles de bolitas incandescentes de metal fundido en el lugar donde se une el acetileno y oxigeno a presión. |
 |
58 El oxigeno es un gas inodoro, incoloro y no tóxico que se encuentra en el aire en un 21% mezclado con nitrógeno, este oxigeno del aire permite que se realicen todos los fenómenos de la combustión , tanto tecnologicos como biológicos. |
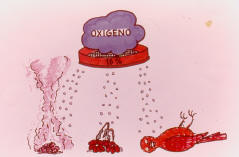 |
59 El oxigeno es un gas comburente necesario para la combustión. Si la proporción del oxigeno del aire se reduce por debajo de un 16% se eliminan los riesgos del fuego pero tampoco es posible la vida. |
 |
60 Si por el contrario aumentaremos la proporci6n de oxigeno, el ambiente llegaría a se explosivo, debido a que una mayor aportación de oxigeno en el aire transforma en inflamables a los combustibles y en combustibles a los que no lo son. |
 |
61 En ocasiones, al oxigeno se le confunde con el aire o viceversa. Operaciones que son normales empleando aire a presión se transforman en muy peligrosas si se utiliza oxigeno. Si un operario limpia el polvo de su ropa con la manguera de oxigeno, es como si la estuviera limpiando con gasolina, una chispa sería suficiente para hacerlo arder. |
 |
62 Emplear oxigeno en presencia de trapos engrasados será causa de su inflamación espontánea, por lo cual nunca se utilizaran aceites o grasa para lubricar los grifos de botellas manoreductores o sopletes. |
 |
63 No se empleará oxigeno para ventilar un local de humo o malos olores el efecto podría ser el mismo como si se intentase ventilar con gas butano. |
 |
64 No se debe emplear oxigeno para destapar tuberías, alimentar herramientas previstas para funcionar con aire comprimido o para trasegar líquidos con su fuerza impulsora. |
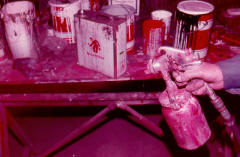 |
65 No se debe emplear oxigeno para pintar a pistola, como elemento de arranque de motores diesel, para hinchar neumáticos, limpiar o desempolvar piezas o activar una combustión, etc. ya que todo ello arrastra graves riesgos de inflamación e incluso de explosión. |
 |
66 El oxigeno para soldar se distribuye en botellas de acero, estando comprimido a I50 o 200 atmósferas de presión. El punto más débil de las botellas suele ser su válvula, la rotura de la cual significa una fuerza de reacción de unos 200 kilos, suficiente para hacer salir disparada la botella como un cohete. |
 |
67 Cuando se utilice la botella de oxigeno, la válvula se abrirá a tope con lo que se evitan fugas el quedar equilibrada la presión en la estopada de la válvula. |
 |
68 Un caudal elevado en el consumo de oxigeno equivale a un enfriamiento de la válvula hasta el extremo que puede quedar impracticable por congelación, en este caso se empleará agua caliente para descongelarla y poder cerrarla, nunca se empleará una llama. |
 |
69 Ante una válvula rebelde que no permita su cierre a apertura, nunca se golpeará o forzará empleando llave alguna, si no es posible accionarla con las manos, lo indicado será avisar al suministrador para que se haga cargo de la misma |
 |
70 Siempre cuando se muevan o transporten las botellas de oxigeno o acetileno de su lugar, se protegerán las válvulas con el capuchón metálico roscado. |
 |
71 El equipo oxiacetilénico compuesto por una botella de oxigeno y otra de acetileno tiene multitud de aplicaciones en la mecánica y en la construcción pudiéndolo encontrar en el más reducido taller metalúrgico. |
 |
72 Estos equipos han de ser manejados por operarios cualificados que dominando las técnicas de corte y soldadura conozcan los riesgos de un uso inadecuado de caudales a sopletes. |
 |
73 Porque además de los riesgos ya mencionados propios de cada componente, tienen un riesgo común en su empleo como es el de provocar incendios en los lugares donde se utilizan, especialmente cuando se realizan trabajos fuera del taller de soldadura. |
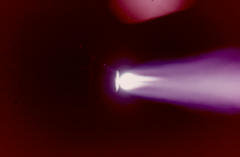 |
74 Generalmente la llama quema en dos fases, la primera fase corresponde a la llama primaria o llama de trabajo donde arde el acetileno y el oxigeno produciendo un dardo blanco y brillante ofreciendo una temperatura de 3.120 grados centígrados y desprendiendo monóxido de carbono e hidrógeno. |
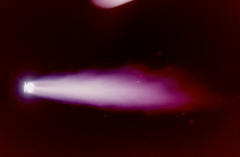 |
75 Alrededor de la llama primaria, se forma el penacho azulado de la llama secundaria, donde el monóxido de carbono e hidrógeno desprendido queman con el oxigeno del aire ambiente ofreciendo una temperatura aproximada de 2.200 grados. |
 |
76 Cuando se realizan soldaduras en pequeñas cavidades o tuberías, el monóxido de carbono e hidrógeno se infiltran en las mismas y no producen llama secundaria hasta entrar en contacto con el aire exterior. Si los gases se enfrían en el interior del tubo forman una mezcla que puede ser explosiva. |
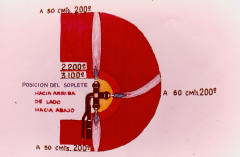 |
77 A le llama secundaria le siguen temperaturas invisibles formadas por anhídrico carbónico, vapor de agua y aire sobrecalentado cuya extensión varia según la posición del soplete y que puede ser causa de fuego en los combustibles cercanos. |
 |
78 Otro riesgo de incendio lo constituyen las proyecciones de metal líquido que se esparcen alrededor del lugar de trabajo y que pueden provocar la ignición de substancias inflamables o combustibles a considerable distancia. |
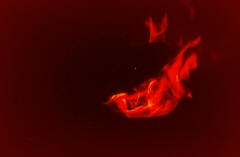 |
79 También pueden introducirse en pequeñas ranuras a agujeros formando pequeños focos de incandescencia o fuegos que no producen llamas hasta pesado bastante tiempo. |
 |
80 Los metales son buenos conductores de calor. Un tubo metálico puede conducir el calor absorvido en el punto de soldadura hasta un punto alejado fuera de la vista del soldador y provocar así la ignición de materias combustibles. |
 |
81 Antes de iniciar el trabajo se rellenará el Permiso de Fuego, formulario obligatorio a rellenar cuando se realizan trabajos de soldadura por gas o arco eléctrico fuera del taller mecánico, en él se indican las normas de prevención a seguir. |
 |
82 Los agujeros a rendijas en paredes, suelo o techo cercanos al lugar de trabajo, se taparan con materiales incombustibles como amianto, yeso barro, mortero, etc. así como las extremidades de los tubos que reciban calor y pueden conducirlo a locales contiguos. |
 |
83 Se apartarán del lugar de trabajo todos los objetos combustibles incluido el polvo. Cuando ello no sea posible se protegerán con revestimientos incombustibles, esteras o mantas de amianto mojadas. |
 |
84 Se tendrá preparado un extintor portátil e incluso según el lugar se tendrá extendida y preparada una manguera de incendios. |
 |
85 Cuando se trabaje en lugares con riesgo de incendio se dispondrá de un ayudante que pueda vigilar las proyecciones de chispas. |
 |
86 De vez en cuando se han de mojar o regar las zonas donde se concentren las chispas o calor, a pesar de estar protegidas pueden acumular suficiente temperatura para provocar fuego. |
 |
87 Una vez terminado el trabajo se examinará la zona, locales, canales a rincones situados el lado, arriba y debajo del lugar verificando que no existe foco de incandescencia, olor a quemado a formación de humo. |
 |
88 La zona continuará en observación durante varias horas y no se pondrán los materiales combustibles en su sitio hasta el día siguiente. |
 |
89 Si ha de realizar un trabajo a fuego libre y tiene dudas en cuanto a la seguridad del lugar, expóngalas a su superior o al propietario del edificio, no improvise pera ganar tiempo, porque el tiempo mejor empleado es el que se destina a la seguridad de personas y bienes. |
 |
90 Silencio Números de teléfono. |
 |
91 Silencio Monumento a los Bomberos. |
|
Antonio Zapater Oliver Miembro del Cuerpo de Bomberos Instructor de Seguridad en Riesgos de Incendio |